۷۵ درصد ژنوم انسان بیمصرف است!
بیگ بنگ: نتایج مطالعهای جدید نشان میدهد دستکم سه چهارم از ژنوم انسان از دیانای غیرکاربردی و بیمصرف تشکیل شدهاست که دانشمندان آن را دیانای زباله نامیدهاند.
اپی ژنتیک چیست؟
بیگ بنگ: اگر خواننده مطالب علمی به خصوص فرگشت و ژنتیک باشید، اصطلاح اپی ژنتیک را چندین بار شنیده اید. اینجا ما سعی داریم تا به زبان ساده و قابل فهم این موضوع را برای شما شرح دهیم. اپی ژنتیک علم نوپایی است اما نقش و اهمیت آن کمتر از خود علم ژنتیک نیست. بسیار خب، اپی ژنتیک چیست؟
به گزارش بیگ بنگ، اپی ژنتیک در لغت به معنای “ورای ژنتیک” است و در این زمینه به بیان یا عدم بیان ژن های ما پرداخته می شود. بگذارید با یک مثال بحث را آغاز کنیم. دوقلوهای همسان از یک DNA شکل می گیرند و به همین دلیل دارای DNA کاملا مشابه هستند. اما خیلی اوقات این دوقلوها در بزرگسالی تفاوت های ظاهری و فیزیکی متفاوتی از هم پیدا می کنند، حتی در خصلت هایی که بنیان ژنتیکی مشابه دارند.
به عنوان مثال: یکی از دو قلوها ممکن است در سن ۵۵ سالگی به بیماری های قلبی دچار شود، در حالی که خواهر دوقلوی او با سلامت کامل در دوی ماراتن شرکت می کند. چرا این اتفاق می افتد در حالی که این دو دارای DNA کاملا یکسان هستند؟ تربیت ممکن است اثر گذار باشند اما جواب اصلی ما در زمینه ای به نام اپی ژنتیک نهفته است. در علم اپی ژنتیک یعنی اینکه چگونه تعداد و تراکم مولکول های کوچک تر در سلول، روی DNA اثر می گذارد. این مولکول ها میتوانند ژن های موجود در DNA را فعال یا غیر فعال کنند. این مولکول ها را به یاد داشته باشید. اگر DNA ما یک کتاب آشپزی باشد، این مولکول ها تصمیم می گیرند که کدام مواد و در چه زمانی پخته شوند. البته این مولکول ها تصمیمات آگاهانه نمی گیرند، بلکه تعدد و تراکم آنها در سلول باعث میزان و نحوه اثر گذاری آنها می شود.
اما چگونه؟
ژن های DNA باید”بیان” بشوند. یعنی باید خوانده شوند و به RNA پیامرسان کپی شوند تا این RNA در خارج از سلول با کمک ریبوزوم شروع به تولید پروتئین کند. این پروتئین های ساخته شده هستند که خصوصیات و عملکرد هر سلول را تعیین می کنند. تغییرات اپی ژنتیکی می توانند بیان یک ژن را بهینه سازند یا در آن مداخله ایجاد کنند. یکی از روش های معمول این نوع مداخله این است که، DNA یا پروتئینی(به نام هیستون) که DNA به دورش پیچ خورده، با برچسب ها شیمیایی کوچک برچسب بخورد. مجموعه ی تمام برچسب هایی که به ژنوم یک سلول متصل اند “اپی ژنوم” آن نام دارند.
بعضی از این برچسب ها مانند گروه های متیلی، از بیان ژن جلوگیری می کنند. حال یا به وسیله تداخل در مولکول کپی کننده DNA به RNA، یا اینکه باعث می شود DNA به دور هیستون محکم تر و تنگ تر پیچ بخورد، که باعث می شود این قسمت از DNA قابل دسترس نباشد. ژن مورد نظر آنجاست ولی فعالیتی ندارد چون ترجمه نمی شود. بهینه سازی کپی و ترجمه ژن توسط این برچسب ها دقیقا برعکس است. یعنی که این برچسب ها باعث می شوند DNA به دور هیستون باز تر شود و در نتیجه راحت ترجمه و کپی شود و پروتئین مربوط به آن ژن بیشتر و بهتر تولید می شود.
تغیرات اپی ژنتیکی می توانند بعد از تقسیم سلول نیز باقی بمانند، این یعنی این تغیرات می توانند از تولد تا مرگ یک موجود روی آن تاثیر بگذارند. بعضی وقتها این تغییرات خوب و جزء رشد و تغیرات عادی بدن موجودات هستند. مثلا سلول های بنیادی در یک رویان همگی دارای یک ژنوم واحد هستند. وقتی که این سلول ها تقسیم می شوند، بعضی از ژن های آنان فعال و بعضی دیگر غیرفعال می شوند. در طول زمان این تغیرات باعث می شود که گروهی از سلول ها بنیادی به سلول های قلب یا سلول های کبد تبدیل شوند و این گونه است که بافت های مختلف سلولی بدن از یک ژنوم مشترک پدیدار می شوند. هر کدام از ۲۰۰ نوع سلول های بدن شما ژنوم یکسان، ولی هر کدام اپی ژنوم مختص خود را دارند.
اپی ژنتیک همچنین باعث می شود که محیط و ژنوم شما تاثیرات متقابل داشته باشند. برچسب هایی که ژن ها را روشن و خاموش می کنند، خود تحت تاثیر تغیرات محیطی مانند: رژیم غذایی، آلودگی های شیمیایی و داروها قرار می گیرند. این تغیرات ممکن است که به بیماری و اختلال های زیستی منجر شوند. به عنوان مثال، یکی از این برچسب ها میتواند ژنی را خاموش کند که مسئول تولید پروتئین مقابله با تومور باشد.
تغییرات اپی ژنتیکی که به وسیله محیط ایجاد می شوند یکی از دلائلی است که چرا دوقلوها در بزرگسالی دارای تفاوت های زیستی می باشند. با بزرگتر شدن دو قلو ها اپی ژنوم آنها نیز متفاوت می شود که باعث می شود روند پیری و مقاومت بر برابر بیماری آنها نیز نسبت به دیگری تغییر کند. حتی تجربیات اجتماعی شما می توانند اپی ژنوم شما را دستکاری کند. در یک آزمایش معروف وقتی که موش های مادر به فرزندان خود بی توجه بودن، ژن هایی که باعث مبارزه در مقابل استرس بودند در این فرزندان خاموش شد.
بیشتر تغیرات اپی ژنتیکی در تشکیل(گامت) سلول ها جنسی پاک می شوند، ولی تحقیقات جدید نشان داده که تعدادی از این برچسب ها باقی میمانند و به نسل های بعدی منتقل می شوند. به عبارتی اپی ژنوم شما قابلیت موروثی بودن را دارد. تجربیات والدین شما در کودکی یا تصمیماتشان در بزرگسالی میتواند اپی ژنوم شما را شکل بدهد. البته خوبی اپی ژنوم این است که دائمی نیست و با یک روش زندگی سالم شما می توانید اپی ژنوم خود را در تعادل و سلامت نگه دارید. تحقیقات و پژوهش های علمی در این زمینه بسیار مهیج و کاربردی اند. چرا که با درک بهتر اپی ژنتیک ما می توانیم چرایی پیری، ایجاد سرطان و خیلی مشکلات و فعالیت های بدن را درک کنیم. با فهمیدن اینکه چگونه اپی ژنتیک، ما را کنترل می کند ما نیز میتوانیم آن را کنترل کنیم.
ترجمه: فرهاد نامجو (دانشجوی کارشناسی مترجمی از دانشگاه باهنر کرمان)
منبع: http://bigbangpage.com/science-content
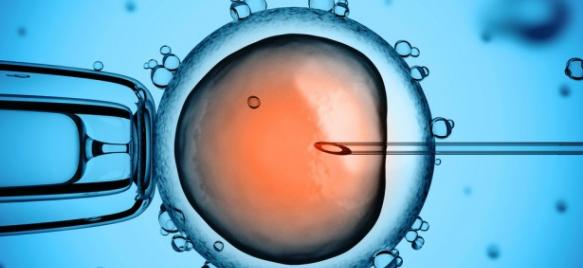
لقاح خارج رحمی (IVF) چیست؟ (ویدئو)
حدود ۱۰-۱۵ درصد زوجها نابارور هستند و در اغلب موارد نیاز است از روشهای کمک باروری -که در اصطلاح علمی به آنها (Assisted Reproductive Techniques)ART میگویند- استفاده شود. روشهای کمک باروری انواع بسیار زیاد دارند که از بسیار ساده شروع و به بسیار پیچیده ختم میشوند. باید دانست که هر زوجی نیازهای مخصوص به خودشان را دارند و باید روش مناسب همان زوج را به آنها پیشنهاد کرد.
IVF مانند IUI یکی از روشهای کمک باروری (ART) است. برخلاف آی یو آی (IUI) که در آن اسپرمهای مرد توسط لولهای وارد رحم خانم میشوند، در آی وی اف (IVF) تخمک خانم با اسپرم مرد در خارج از بدن، در محیط آزمایشگاه باهم ترکیب میشوند و پس از لقاح، جنین حاصله در داخل رحم خانم گذاشته میشود. از زمان تولد اولین نوزاد با استفاده از روش درمانی IVF در سال ۱۹۷۸، این روش درمانی، امید تازهای برای زوجهای نابارور به وجود آورده است. IVF مخفف اصطلاح In Vitro Fertilization یا لقاح خارج رحمی است.
در تمام مواردی که شرایط رسیدن اسپرم به تخمک در رحم فراهم نباشد مانند بسته بودن لولههای رحمی، چسبندگیهای حفره لگنی، تعداد کم اسپرم و تحرک پایین اسپرم از روش IVF استفاده میشود. میزان موفقیت IVF برای هر انتقال جنین در مراکز درمان ناباروری، بر اساس شرایط آزمایشگاه جنین شناسی و دقت متخصصین زنان در روند درمان، همچنین وضعیت اسپرم و تخمک و سن زن مورد ارزیابی قرار میگیرد. با توجه به شرایط گوناگون، میزان موفقیت در هر بار انجام عمل انتقال جنین متفاوت است و معمولاً بین ۳۰-۴۰ درصد میباشد.
برای مشاهده متن کامل این پست به ادامه مطلب (بر روی فلش قرمز رنگ سمت چپ کلیک نمایید) مراجعه فرمایید
جهت مشاهده این ویدئو و سایر ویدئوهای وبسایت به کانال تلگرام بیوسای مراجعه فرمایید
ساخت سلولهای «ضربانساز» قلب از سلولهای بنیادی (ویدئو)
ساخت سلولهای ضربان ساز قلب از سلول های بنیادی
راهی برای درمان ماندگار قلب هایی که ضربان ضعیف دارند
جهت مشاهده این ویدئو و سایر ویدئوهای آموزشی وبسایت به کانال تلگرام بیوسای مراجعه فرمایید
چرا زنان و مردان متفاوت می اندیشند؟
⬅️ تصور بر آن است که، کروموزوم هایی که در تعیین جنسیت نقش دارند، در طی تکوین، حین تشکیل سایر اندام ها نیز دخالت هایی می کنند.
⬅️ کروموزم Y کرچه کروموزم کوچکی است اما شناخت فعالیت آن در مراحل مختلف تکوین توانسته است به سوالات متعددی پاسخ دهد.
⬅️ در پروژه جهانی پروتئوم انسانی که کشور های متعدد در کنار هم به بررسی بیان پروتئین های کروموزم های انسانی می پردازند، پژوهشگاه رویان از ایران مسئول رمز گشایی از پروتئین هایی است که توسط کروموزم Y بیان می شوند.
⬅️ به دنبال یافتن نقش کروموزم Y در تکوین دستگاه عصبی مردان، در پژوهشگاه رویان و دانشگاه سیدنی استرالیا، نشان دادند در حین تکوین دستگاه عصبی مردان بخشی از کروموزم Y و 15 ناحیه وابسته به آن در کروموزم X فعال می شوند و با تولید پروتئین هایی در شکل گیری این اندام دخالت می کنند.
🔷🔶 نتایج این پژوهش نشان داد، طی تمایز سلول های عصبی میزان بیان 12 ژن وابسته به کروموزم Y به شکل معنی داری افزایش می یابد (ژن هایی مانند RBMY1, ELF1AY, DDX3Y, HSFY1).
🔷🔶 همچنین در این پژوهش نشان داده شد اگر ژن DDX3Y به وسیله RNAهای کوچک مداخله کننده مهار شود مرگ برنامه ریزی شده سلولی در سلول های عصبی در حال تمایز مذکر القا شده تمایز مختل می شود.
🔺🔻 این یافته نشان می دهد DDX3Y نقش مهمی در تکوین سلول های عصبی مردان داشته اختلال در آن تکوین عصبی را در این جنس دچار مشکل می کند.
از DNA تا پروتئین (+ویدئو)
From DNA to Protein
فرآیند پروتئین سازی در سلول
دانش آموزان عزیز برای درک بهتر این ویدئو فصل 1 زیست پیش دانشگاهی را مطالعه نمایید
جهت مشاهده ویدئو وارد کانال تلگرام بیوسای شوید
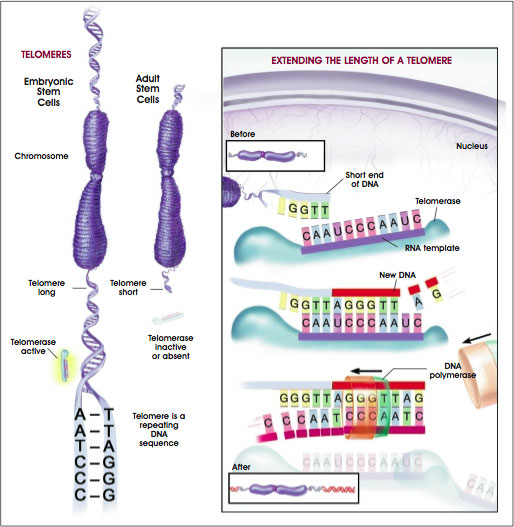
اهمیت بیولوژی تلومر، تلومراز و ارتباط آن با فرآیند پیری (+ویدئو)
فنیل کتونوری (PKU)
PKU که مخفف عبارت PHENYL KETONURIA فنیل کتونوری است ، ازجمله بیماری های ژنتیکی است که به علت کمبود نوعی آنزیم در کبد نوزادان به وجود می آید. چون در ادرار مبتلایان ماده ای به نام فنیل کتون وجود دارد به همین دلیل بیماری را فنیل کتونوری نامیده اند.
بیماری پی کی یو نوعی اختلال ارثی است که از پدر و مادر به فرزند منتقل می شود. نوزاد مبتلا به علت کمبود آنزیم مخصوصی در کبد خود، قادر به هضم فنیل آلانین نیست.
فنیل آلانین که به طور خلاصه «فی» خوانده می شود، جزو مواد ضروری در سلامت انسان است. این ماده در ترکیب پروتئین ها موجود است و با غذا وارد بدن می شود.در نوزادان مبتلا به این بیماری مصرف غذاهای پروتئینی از جمله شیر مادر و یا شیر خشک معمولی باعث افزایش شدید غلظت خونی «فی» و تجمع آن در بافت های مختلف بدن می شود و رشد و تکامل مغز و اعصاب را مختل می کند و به ضایعه مغزی و یا عقب ماندگی ذهنی پایدار منجر می شود.
این بیماری در بدو تولد هیچ گونه نشانه بارزی ندارد و نوزاد در ۲ تا ۳ ماه اول زندگی ظاهر کاملا سالمی دارد ولی به تدریج علایمی هم چون بی میلی به خوردن شیر، استفراغ بعد از خوردن شیر، بروز اگزما و جوش در سطح بدن، بورشدن موهای سر بدون سابقه ارثی ظاهر می شود.عرق بدن و ادرار این نوزادان اغلب بوی زننده و بسیار نامطبوع کپک مانند دارد.با گذشت زمان کودک دچار عقب ماندگی ذهنی می شود. این کودکان اغلب ناآرام و پرجنب و جوش اند و تعادل عصبی خوبی ندارند.قدرت تکلم این کودکان ضعیف و راه رفتن آن ها دچار مشکل می شود که ممکن است برای همیشه باقی بماند.
تظاهرات بالینی بیمار تا ۶- ۵ ماهگی بسیار گمراه کننده است. متاسفانه تشخیص اغلب ، زمانی اتفاق می افتد که بیماری منجر به عقب ماندگی ذهنی کودک شده است و ضایعه مغزی به وجود آمده درمان ناپذیر شده است.بنابراین تنها و بهترین راه تشخیص این بیماری اندازه گیری غلظت خونی «فی» در بدو تولد نوزاد است.این آ زمایش باید هرچه زودتر در روزهای اول تولد انجام شود، زیرا تاخیر در تشخیص بیماری از هفته سوم به بعد خطرناک است و ممکن است صدمات مغزی به معلولیت دائم منتهی شود.
آزمایش روی قطره خونی که از پاشنه پای نوزاد گرفته می شود، انجام می گیرد. روش خون گیری، بسیار ساده و بدون ضایعه است به این ترتیب که با وارد کردن یک سوزن ظریف و مخصوص (لانست) به پاشنه پای نوزاد ۲ تا ۳ قطره خون روی کاغذ صافی مخصوص می چکانند و بعد از خشک شدن کامل خون، کاغذ صافی برای انجام آزمایش به آزمایشگاه ارسال می شود.
باید در نظر داشت که مثبت بودن نتیجه آزمایش همیشه دلیل بر ابتلای نوزاد به بیماری نیست، زیرا ممکن است کبد بعضی از نوزادان به خصوص آن هایی که نارس به دنیا آمده اند، در روزهای اول تولد هنوز به طور کامل فعال نشده باشد، در نتیجه«فی» خون آن ها به طور طبیعی افزایش نشان می دهد.ولی چند روز بعد با رشد نوزاد، فعالیت کبد به وضع طبیعی بر می گردد و نتیجه آزمایش اصلاح می شود بنابراین در این شرایط تمام آزمایش ها بعد از ۷ تا ۸ روز باید دوباره تکرار شود تا نتیجه اول تایید شود.در این مدت و تا مشخص شدن نتیجه نهایی نباید نوزاد را از شیر مادر یا غذای متعارف محروم کرد. جواب طبیعی در مرحله اول و یا دوم نشانه سلامت نوزاد است. ولی نتیجه مثبت در هر ۲ نوبت دلیل بر این است که نوزاد باید تا مدتی تحت نظر متخصص کودکان و کارشناس تغذیه قرار گیرد و با رژیم غذایی مخصوص مداوا شود.
منبع:
http://www.genetic-center.ir/
سندرم داون (Down Syndrome)
سندرم داون که در گذشته مونگولیسم نیز نامیده میشد، یک بیماری ژنتیکی است که به دلیل افزایش تعدادی کامل یا نسبی در کروموزم ۲۱ به وجود میآید. این بیماری دارای علایم مختلف از جمله ناهنجاریهای عمده و یا خفیف در ساختار یا عملکرد ارگانها میباشد. از جمله علایم عمده و زودرس که در تقریباً همه بیماران مشاهده میشود وجود مشکلات یادگیری و نیز محدودیت و تاخیر رشد و نمومیباشد.
نام این سندرم از نام یک پزشک انگلیسی به نام جان لانگزدان داون (John Langsdon Down) گرفته شدهاست که برای اولین بار این سندرم را در سال ۱۸۶۶ توصیف نمود. افراد مبتلا به سندرم داون توان ذهنی پایین تر از حد میانگین دارند و به طور معمول دچار ناتوانی ذهنی خفیف تا متوسط هستند. تعداد کمی از مبتلایان به سندرم داون دچار ناتوانی شدید ذهنی هستند. متوسط میزان بروز این سندرم مابین ۱ در ۶۰۰ تا یک در ۱۰۰۰ مورد از تولد نوزادان زنده گزارش شده است که این میزان در مادران جوان کم تر و باافزایش سن مادر افزایش مییابد. با این وجود در حدود دو سوم مبتلایان به سندرم داون از مادران زیر ۳۵ سال متولد میشوند.
در گذشته برای پیشگیری از سندرم داون توصیه میشد که همه مادران بالای ۳۵ سال توسط آزمایش سلولهای مایع آمنیوتیک (آمنیوسنتز) یا نمونهگیری از پرزهای جفتی (CVS) تحت بررسی قرار گیرند. اما از آنجا که بیش از دو سوم نوزادان مبتلا به سندرم داون از مادران زیر ۳۵ سال متولد میشوند در حال حاضر شیوههای غربالگری سندرم داون به همه مادران باردار توصیه میشود.در این شیوهها که معمولاً در سه ماهه اول بارداری یا سه ماهه دوم بارداری انجام میگیرند از روشهای غیر تهاجمی همانند بررسی خون مادر یا سونوگرافیاستفاده میشود.
منبع:
http://www.genetic-center.ir/
تالاسمی چیست؟
تالاسمی از بیماری های ژنتیکی است که بر اثر آن هموگلوبین ساختار طبیعی خود را از دست می دهد؛ بنابراین پدیده تولید هموگلوبین غیرموثر در بدن ایجاد می شود. هموگلوبین معیوب قادر به اکسیژن رسانی مطلوب به اعضای بدن نیست. پس در واقع کمبود کلی هموگلوبین وجود ندارد بلکه هموگلوبین غیرطبیعی افزایش می یابد.هموگلوبین جزو انتقال دهنده اکسیژن در سلول های قرمز خونی است و شامل دو پروتئین مختلف به نام آلفا و بتاست. اگر بدن توانایی تولید کافی از هر نوع پروتئین را نداشته باشد، سلول های خونی به طور کامل شکل نمی گیرد و توانایی انتقال اکسیژن کافی را ندارد که نتیجه آن بروز یک نوع کم خونی است که در طفولیت آغاز می شود و تا پایان عمر به طول می انجامد. تالاسمی به دو نوع آلفا تالاسمی و بتاتالاسمی است. در بتاتالاسمی اختلال روی کروموزوم «۱۱» و در آلفا تالاسمی اختلال روی کروموزوم «۱۶» است. در کشور ما نوع بتاتالاسمی شایع است، بنابراین موضوع بحث ما بتاتالاسمی است. بتاتالاسمی شامل تالاسمی ماژور (تالاسمی شدید) و تالاسمی مینور یا تالاسمی خفیف است.
افراد مبتلا به تالاسمی مینور در واقع کم خونی مشکل سازی ندارند ولی اگر دو فرد تالاسمی مینور با هم ازدواج کنند به احتمال ۳۵ درصد فرزندشان دچار تالاسمی شدید یا ماژور خواهد بود و ۲۵ درصد فرزندشان سالم و ۵۰ درصد تالاسمی مینور خواهند داشت. تالاسمی ماژور یا آنمی کولی به علت حذف یا جهش در هر دو ژن سازنده زنجیره بتا ایجاد می شود و به این ترتیب یا هیچ زنجیره بتایی ساخته نمی شود یا به مقدار کمی ساخته می شود. در نتیجه بدن کمبود این زنجیره ها را با ساخت زنجیره های آلفا جبران می کند که این زنجیره های آلفای اضافی برای گلبول های قرمز سمی است و با رسوب روی سلول های گلبول قرمز باعث می شود که گلبول های قرمز در مغز استخوان و در داخل خون تخریب شود و زنجیره های آلفا در مغز استخوان رسوب کند. از طرفی به علت خون سازی غیرموثر، مراکز خون ساز خارج مغز استخوان، از جمله کبد و طحال شروع به خون سازی می کند و بزرگ می شود. شایع ترین درمان برای تمامی اشکال تالاسمی تزریق سلول های قرمز خونی است. این تزریق خون برای فراهم آوردن مقادیری از سلول های قرمز خونی سالم و هموگلوبین طبیعی که قادر به انتقال اکسیژن باشد، ضروری است. اما همان طور که پیشتر نیز اشاره شد بهترین درمان پیش گیری از وقوع بیماری است. بیماری تالاسمی از اولین رده های پیشتاز بیماری های ارثی در کشور ماست که باید کنترل شود. در حال حاضر موثرترین راه پیش گیری از بیماری تالاسمی غربالگری این بیماری و سپس بررسی مولکولی افرادی است که در غربالگری در گروه افراد تحت خطر طبقه بندی شده اند. برای این منظور در ایران برنامه کشوری غربالگری تالاسمی توسط وزارت بهداشت در حال انجام است. با مشاوره ژنتیک در ازدواج های دو شخص مینور با هم و نمونه برداری از جفت و یا آمنیوسنتز (هفته ۱۰-۱۵ حاملگی) و بررسی DNA در صورتی که تشخیص داده شود که جنین مبتلا به تالاسمی ماژور است سقط صورت خواهد گرفت که اجازه شرعی آن نیز گرفته شده است.
منبع:
http://www.genetic-center.ir/

مجله علمی زیست شناسی
_________________
دانستنیهای زیست شناسی
زیست شناسی دبیرستان و کنکور
ویدئوها و انیمیشن های آموزشی
جزوات و نمونه سوالات
کتب و رفرنس های علمی
مقالات علمی و پژوهشی
__________________
حمید نقی زاده
کارشناس ارشد فیزیولوژی دام
دبیر زیست شناسی دبیرستانها و آموزشگاههای تهران
بایوسای را در آپارات، تلگرام و اینستاگرام نیز دنبال کنید